私たちの脳を支配するのは、脳ではないのかもしれない
これまで、脳の神経細胞が徐々に失われていく難病の原因は、主に加齢や抗えない遺伝子の変異にあると考えられてきました。しかし、最新の科学はその常識に一石を投じています。私たちの思考や運動を司る脳の健康状態を、実は脳から遠く離れた「腸」の住人たちが左右している可能性が浮上したのです。
筋萎縮性側索硬化症(ALS)や前頭側頭型認知症(FTD)という、治療法が確立されていない深刻な神経変性疾患。これらの病の発症プロセスにおいて、腸内細菌がいかにして引き金(トリガー)を引くのか。ケース・ウェスタン・リザーブ大学の研究チームが発表した、既存の医学概念を揺るがす驚くべきメカニズムを解説します。
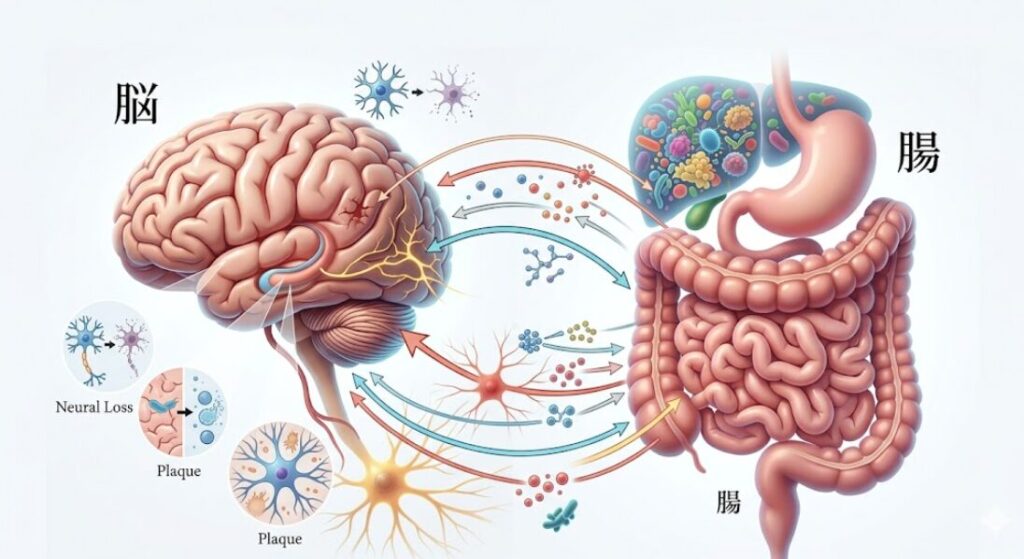
驚きの発見:細菌が作り出す「炎症性シュガー」の正体
今回の研究における最大の発見は、特定の腸内細菌が生成する物質が、脳への「侵攻」を可能にしているという事実です。
研究チームは、腸内細菌の一種である「パラバクテロイデス・メルダエ(Parabacteroides merdae)」などが、特殊な「グリコーゲン(多糖類の一種)」を生成していることを突き止めました。本来、グリコーゲンは生体内のクリーンなエネルギー源として知られていますが、この細菌由来のグリコーゲンは、体内で激しい免疫反応を引き起こす「炎症性」という極めて特異な性質を持っていました。
この発見が衝撃的なのは、グリコーゲンを単なる栄養源ではなく、一種の「病原体」のような振る舞いをする毒性物質として定義し直した点にあります。この「炎症性シュガー」が蓄積すると、本来は有害物質の侵入を防ぐ役割を果たす「血液脳関門(BBB)」の崩壊を招き、炎症が脳へと波及、結果として神経細胞の死を招くというのです。
「有害な腸内細菌が炎症性のグリコーゲンを生成し、それが免疫反応を引き起こして脳にダメージを与えることを発見しました」
アーロン・バーベリー(Aaron Burberry)助教がそう語るように、腸で作られた「糖」が防壁を突き破り、脳を攻撃するという新たな病態ルートが明らかになりました。
遺伝子だけでは決まらない:C9ORF72遺伝子の意外な役割
ALSやFTDの主要な遺伝的要因として、「C9ORF72」という遺伝子の変異が知られています。しかし、この変異を持つ人が必ずしも発症するわけではないという事実は、長らく医学界の謎でした。この謎を解く鍵こそが、腸内細菌との「相互作用」です。
研究の結果、C9ORF72遺伝子から生成されるタンパク質は、細菌由来の炎症性グリコーゲンに対して「ブレーキ」をかけ、抑制する役割を担っていることが判明しました。つまり、以下のようなプロセスで病気が進行します。
- 遺伝的要因(ブレーキの故障): C9ORF72の変異により、炎症性グリコーゲンを抑える力が弱まる。
- 環境的要因(アクセルの暴走): 腸内環境の悪化により、特定の細菌が炎症性グリコーゲンを過剰に生成する。
この「設計図(遺伝子)の不備」と「腸内環境という環境因子」が最悪の形で組み合わさったとき、炎症のブレーキが効かなくなり、脳の変性が加速するのです。単に遺伝子変異があるだけでは発症せず、腸内の「真犯人」が活動を開始して初めて、負の連鎖が完成するという論理的な構図が見えてきました。
マウスから人間へ:裏付けられたデータと今後の展望
このメカニズムは、マウス実験のみならず、実際の患者のデータによっても強力に裏付けられています。
ALS患者22名とFTD患者1名を対象とした調査では、実にそのうちの16名(ALS患者15名とFTD患者1名)の糞便サンプルから、通常よりも高いレベルの炎症性グリコーゲンが検出されました。これに対し、健康な対照群で高いレベルが見られたのは12名中4名に留まっています。
また、希望を感じさせる実験結果も報告されています。炎症を起こしたマウスに、グリコーゲンを分解する酵素「α-アミラーゼ」を投与したところ、体内の炎症レベルが抑制され、寿命を延ばすことに成功しました。ただし、「運動機能の改善には至らなかった」という重要な科学的知見も得られており、この治療法が万能な「完治」を意味するわけではないという冷静な視点も必要です。
しかし、この発見は治療のパラダイムシフトを予感させます。これまで「脳」というアプローチの難しい部位に限定されていた治療ターゲットを、より介入しやすい「腸」へと切り替えられる可能性があるからです。
腸内環境が切り拓く、難病治療の新たな一歩
脳の健康を守る鍵が、実は私たちの腹部の中に隠されているという事実は、現代医学にパラダイムシフトを迫っています。脳の難病を「脳だけの不具合」と捉えるのではなく、全身のシステム、特に腸内細菌との関わりの中で理解する新たなフェーズに突入したのです。
この研究はすでに実用化への第一歩を踏み出しており、バーベリー助教によれば、グリコーゲン分解を標的とした治療の臨床試験は、早ければ1年以内にも始まる可能性があるといいます。
私たちはこれまで、自分の体を一つの独立した個体と考えてきました。しかし、腸内に住む細菌たちが作り出す小さな「糖」が、私たちの脳の運命、ひいては人生の質を左右しているのだとしたら――。今日あなたが選ぶ食習慣やライフスタイルが、腸内環境を通じて数十年後の脳の未来を書き換えているのかもしれない。そんな視点で、自分自身の体を見つめ直してみてはいかがでしょうか。


コメント